如何学好化学这门课
1、元素周期表和元素周期律男帮助我们更好的理骈禄笫杳解化学反应,金属元素及非金属元素的氧化还原能力基本上是按照元素周期律来的,为什么钠比镁更活泼,化学反应更明显等一系列都可以从元素周期律中总结出来。
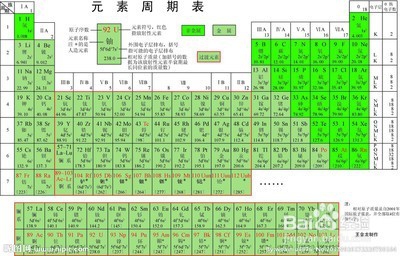
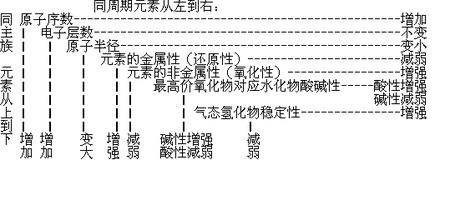
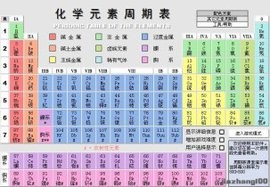
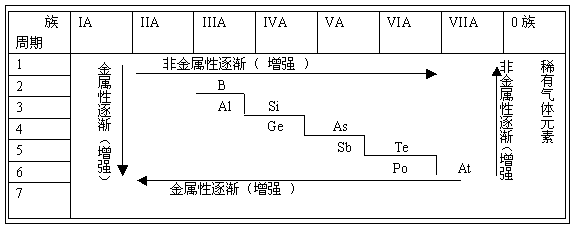
2、元素周期表有7个周期,16个族。每一个横行叫作一个周期,每一个纵行叫作一个族。1:同一周期内,从左到右,元素核外电子层数相同,最外层电子数依次递增,原子半径递减(零族元素除外)。失电子能悝洳合撺力逐渐减弱,获电子能力逐渐增强,金属性逐渐减弱,非金属性逐渐增强。元素的最高正氧化数从左到右递增(没有正价的除外),最低负氧化数从左到右递增(第一周期除外,第二周期的O、F元素除外)2:同一族中,由上而下,最外层电子数相同,核外电子层数逐渐增多,原子序数递增,元素金属性递增,非金属性递减。
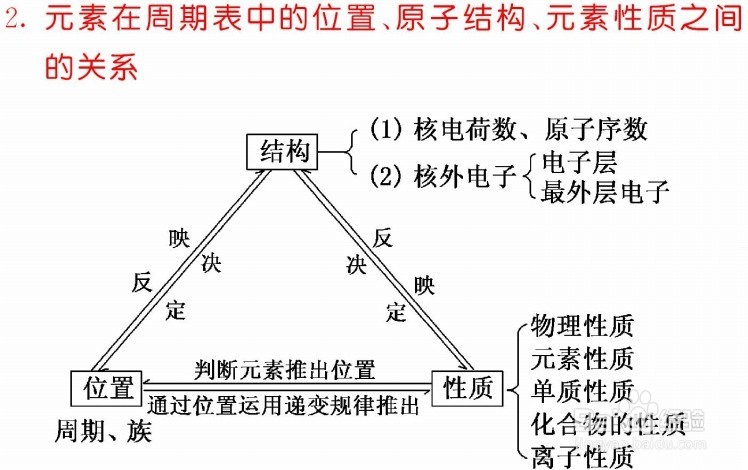
3、元素在周期表中的位置、原子结构、元素性质之间的关系。例如:原子半径由左到右依次减小,上到下依次增大。
4、按照元素在周期表中的顺序给元素编号,得到原子序数。原子序数跟元素的原子结构有如下关系:质子数=原子序数=核外电子数=核电荷数
5、元素的金属性越强,其第一电离能就越小;非皙祛土耘金属性越强,其第一电子亲和能就越大。 同一周期元素中,轨道越“空”的元素越容易失去电子,轨道越“满”的越容易得电子等规律。
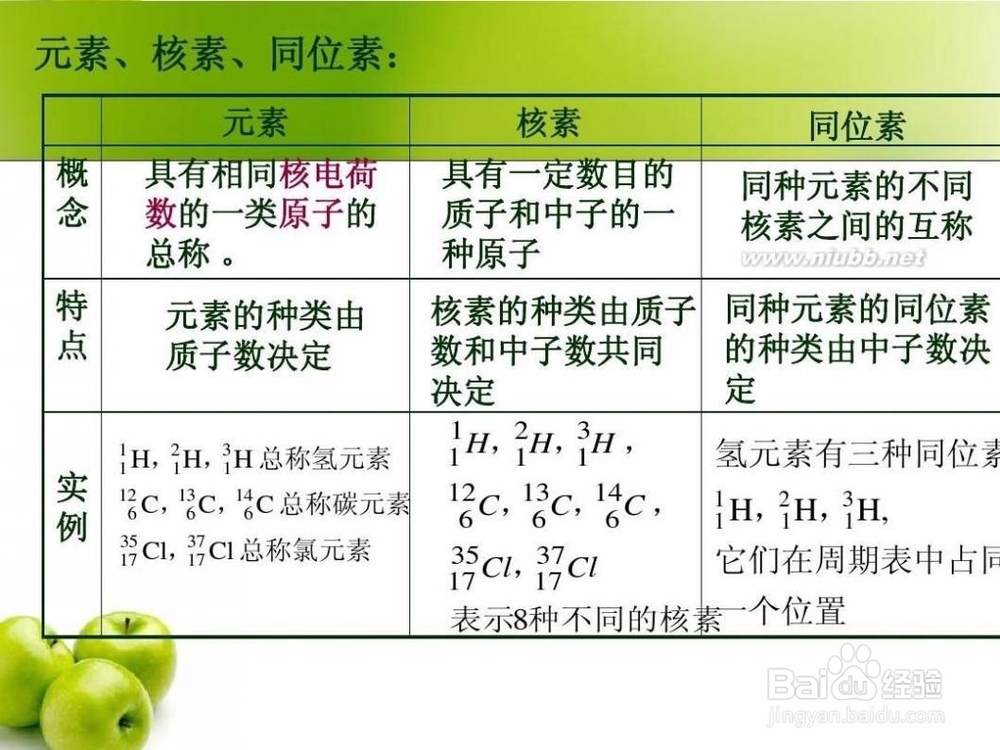
6、元素、荷数以及同位素的概念
声明:本网站引用、摘录或转载内容仅供网站访问者交流或参考,不代表本站立场,如存在版权或非法内容,请联系站长删除,联系邮箱:site.kefu@qq.com。