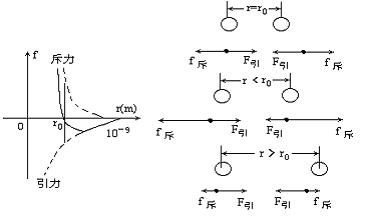
分子间为什么有斥力和引力
因为原子核里面有质子。外面有电子。质子带正电。电子带负电。在正常情况下正负电荷相等。所以对外不表禊耗髻编现出电荷。那么分子里面存在大量的原子。原子与原子间由于外面的电子层互相会有一个排斥力。而内部正负会相吸。
所以引力斥力都有。分子间存在着引力,可由下列事实说明:固体能保持一定的形状和体积,要把固体的一部分跟另一部分分开是很困难的.液体虽然没有一定的形状,但也有一定的体积。
分子之间存在着间隙,但液体、固体很难压缩,这说明分子间存在着相互作用的斥力。分子间的引力和斥力是同时存在的,它们的大小都跟分子间的距离有关。当分子处于平衡位置时,分子所受的引力和斥力相互平衡,合力为零。
当分子间距离小于10-10米时,分子间的作用力表现为斥力,由二力合成知识可知,即合力方向与斥力方向相同。
当分子间距离大于10-10米时,分子间的作用力表现为引力,即分子所受的引力和斥力的合力方向与引力相同。当分子间距离大于分子直径10倍时,分子间作用力变得十分微弱,以致可以忽略了。
扩展资料:
分子间作用力只存在于分子(molecule)与分子之间或惰性气体(noble gas)原子(atom)间的作用力,又称范德华力(van der waals),具有加和性,属于次级键。
氢键(hydrogen bond)、弱范德华力、盐键、疏水作用力、芳环堆积作用、卤键都属于次级键(又称分子间弱相互作用)。
作用力分类
定义:范德华力(又称分子作用力)产生于分子或原子之间的静电相互作用。其能量计算的经验方程为:U =B/r12- A/r6 (对于2 个碳原子间,其参数值为B =11.5 ×10-6 kJ·nm12/mol ;A=5.96 × 10-3 kJnm^6/mol;不同原子间A、B 有不同取值)当两原子彼此紧密靠近电子云相互重叠时,发生强烈排斥,排斥力与距离12 次方成反比。
低点是范德华力维持的距离作用力最大,称范德华半径。分子引力与距离6次方成反比,分子斥力与距离12次方成反比。
范德华力又可以分为三种作用力:诱导力、色散力和取向力。
参考资料:百度百科-分子间作用力